§ 2. Строение атома и периодический закон
1. В ядрах атомов химических элементов содержится соответственно 9, 24, 38, 78 и 86 протонов. Назовите эти элементы. Укажите их «адреса» в периодической системе элементов.
Z = 9 → Фтор (F): 2 период, 17 группа (VIIA).
Z = 24 → Хром (Cr): 4 период, 6 группа (VIB).
Z = 38 → Стронций (Sr): 5 период, 2 группа (IIA).
Z = 78 → Платина (Pt): 6 период, 10 группа (VIII по старой системе).
Z = 86 → Радон (Rn): 6 период, 18 группа (VIIIA).
2. Определите атомный номер элемента, у которого массовое число атома равно 26, а число нейтронов в ядре — 14.
Атомный номер: Z = A − N = 26 − 14 = 12 (это Mg).
3. Укажите состав атомных ядер изотопов:

4. Как современная атомная теория описывает состояние электрона в атоме?
Современная теория не приписывает электрону в атоме определённой траектории. Его состояние описывается вероятностно – как электронное облако вокруг ядра; область наибольшей вероятности нахождения называется атомной орбиталью. Электрон при этом характеризуется энергией и спином.
5. Составьте электронные схемы атомов азота, магния, алюминия, фосфора, аргона.
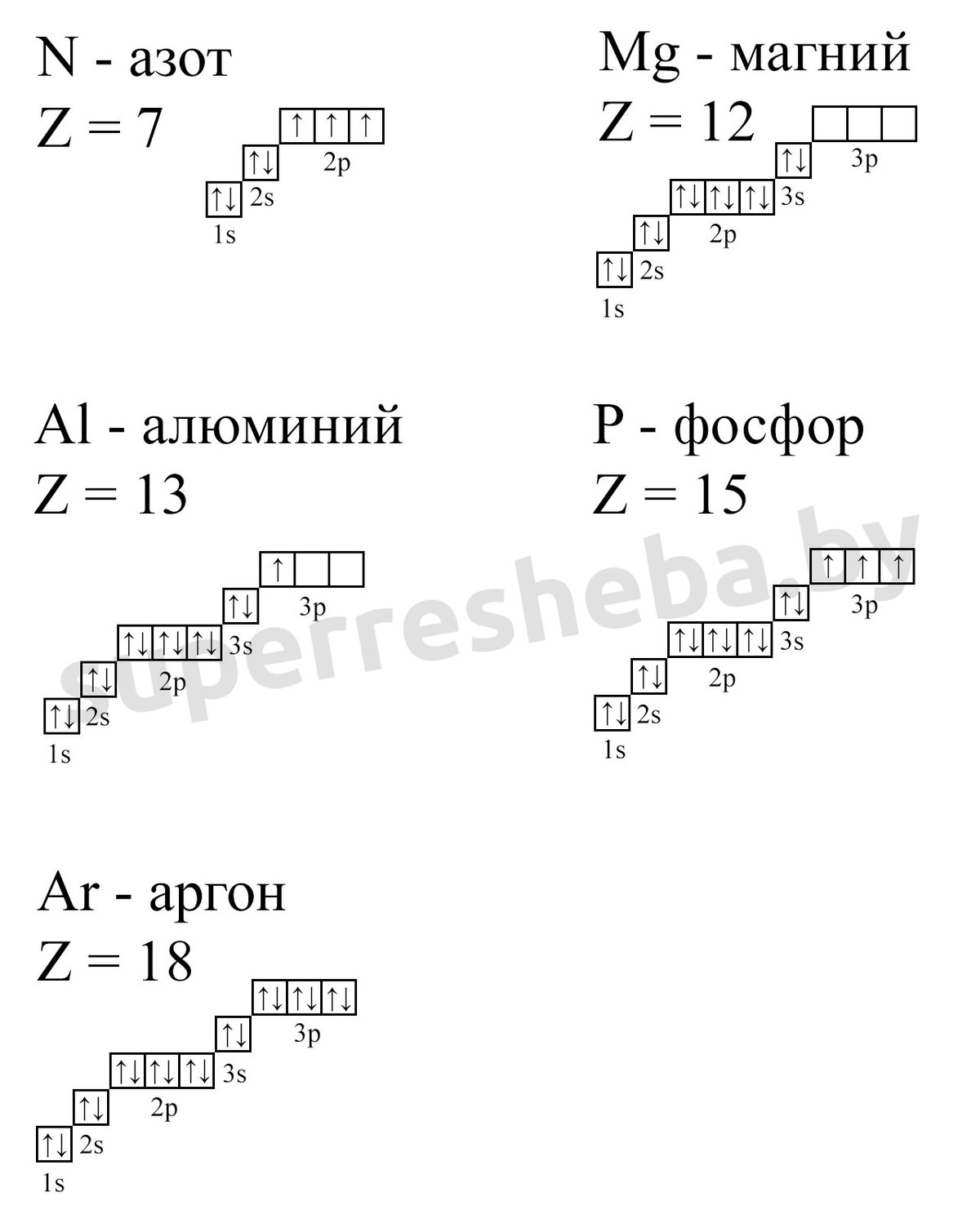
6. Что является причиной периодичности свойств атомов химических элементов?
Периодичность свойств обусловлена периодическим повторением строения внешних (валентных) электронных уровней атомов при возрастании атомного номера.
7. Как изменяются свойства высших оксидов и соответствующих им гидроксидов в группах и периодах? Составьте их формулы для элементов IVА-группы и третьего периода.
В группах: С возрастанием атомного номера элемента (сверху вниз) усиливаются основные свойства оксидов и гидроксидов, а кислотные свойства ослабевают.
В периодах: С ростом зарядов ядер атомов (слева направо) свойства оксидов и гидроксидов изменяются от основных к кислотным.
IVA-группа
C: CO2 → H2CO3
Si: SiO2 → H2SiO3
Ge: GeO2 → Ge(OH)4 (также H2GeO3)
Sn: SnO2 → Sn(OH)4
Pb: PbO2 → Pb(OH)4
Третий период
Na: Na2O → NaOH
Mg: MgO → Mg(OH)2
Al: Al2O3 → Al(OH)3
Si: SiO2 → H2SiO3
P: P2O5 → H3PO4
S: SO3 → H2SO4
Cl: Cl2O7 → HClO4
Ar: не образует устойчивых оксидов и гидроксидов
8. Напишите уравнения реакций высших оксидов калия, кальция, фосфора и углерода с водой.
K2O + H2O → 2KOH
CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4
CO2 + H2O ⇄ H2CO3