Лаб. 2
1.
Раствор вещества – хлороводородная кислота
Реактив – нитрат серебра (I)
На рисунке:
левая пробирка – HCl
верхняя пробирка – AgNO3
правая пробирка – AgCl
Признак реакции: выпадение белого осадка хлорида серебра (I).
Раствор вещества – хлорид натрия
Реактив – нитрат серебра (I)
На рисунке:
левая пробирка – NaCl
верхняя пробирка – AgNO3
правая пробирка – AgCl
Признак реакции: выпадение белого осадка хлорида серебра (I).
2.
Минеральная вода совсем немного помутнела. Это значит, что в минеральной воде есть хлорд-ионы.
3.
а)
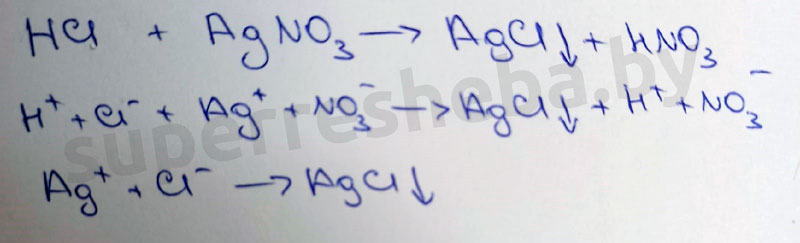
б)

Вывод
Обнаружить хлорид-ионы в растворах можно при помощи нитрата серебра (I) – это качественная реакция на ионы хлора. Выпадение осадка обусловлено связыванием ионов хлора с ионами серебра, которые вместе образуют нерастворимый осадок.
Задания
1. CO32-, Cl-, NO3-, K+, I- , Br-
2. H+, Cl-, Na+, F-
3.
Ион хлора:
г) в растворах можно обнаружить по реакции с ионами серебра
4. ... ионами серебра образует ... Это Cl-.
5.
В раствор добавим нитрат серебра (I). В результате произойдет реакция между нитратом серебра (I) и хлоридом натрия. В результате выпадет осадок хлорида серебра (I). В растворе останется соль нитрата натрия.