Лаб. 13
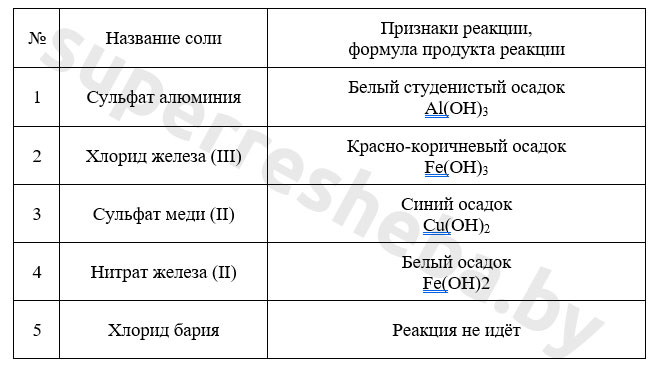
1. Налейте в одну пробирку раствор хлорида железа (III), а во вторую – сульфата железа (II) объемом примерно 1-2 см3. Прибавьте к растворам по несколько капель раствора гидроксида натрия. Отметьте цвет выпавших осадков, запишите формулы продуктов реакции в таблицу.

Уравнение химических реакций обнаружения ионов железа в молекулярном и ионном виде:
а) б)
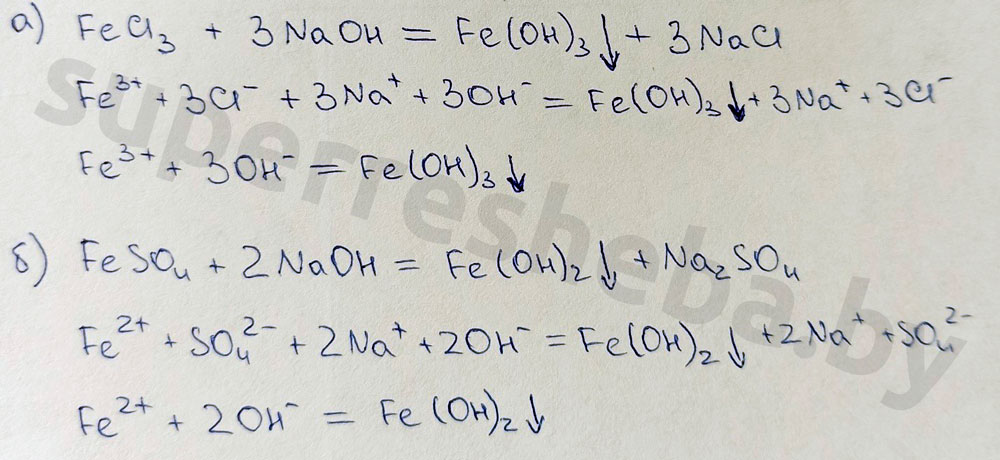
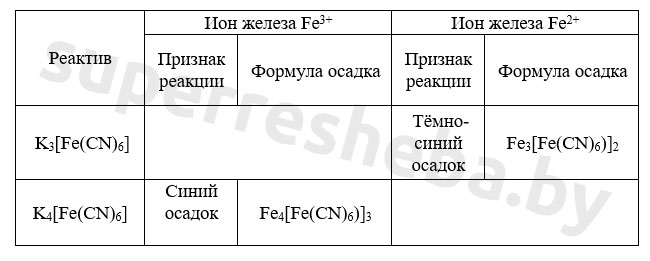
2. Проведите качественные реакции на ионы железа в растворе с красной и желтой кровяными солями. В две пробирки налейте растворы солей железа: в первую – сульфата железа (II), во вторую – хлорида железа (III). В первую пробирку добавьте 2-3 капли разбавленного раствора гексацианоферрата (III) калия, а во вторую – столько же гексацианоферрата (II) калия. Отметьте цвет образовавшихся осадков. Результаты наблюдений занесите в таблицу:
Однако по новым данным в результате реакции с образуется Ранее считалось, что при этом образуется гексацианоферрат (III) железа (II), то есть именно такую формулу предлагали для «турнбулевой сини». Теперь известно, что турнбулева синь и берлинская лазурь — одно и то же вещество, а в процессе реакции происходит переход электронов от ионов к гексацианоферрат (III)-иону.
Уравнения химических реакций в молекулярном виде, назовите продукты реакций:

3. Сделайте вывод об условиях и признаках протекания качественных реакций на ионы железа (II) и (III) в растворе.
В результате качественных реакций на ионы железа со щелочью мы наблюдаем выпадение бурого осадка гидроксида железа (III) и белого осадка гидроксида железа (II). А в результате реакций с гексацианоферратами калия образуются осадки синего цвета: турнбулева синь и берлинская лазурь. Все реакции протекают в растворе или расплаве.
4. Задания.
1.
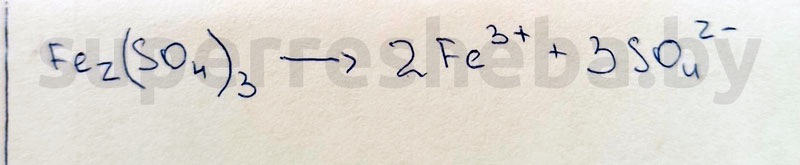
2.
+2 – FeO
+3 – Fe2O3
+6 – H2FeO4 (в свободном виде не существует)
3.

4.
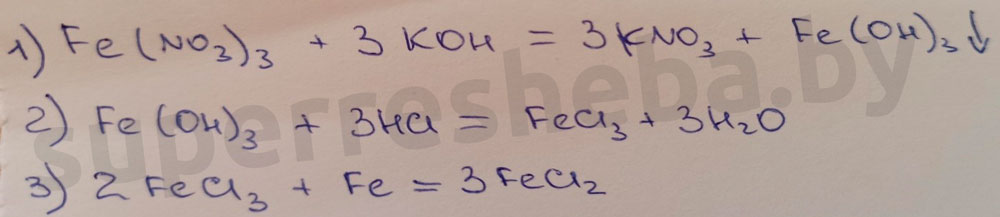
5.