§ 38. Углеводы. Глюкоза
1. Приведите примеры использования глюкозы.
Глюкоза применяется в медицине, в производстве лимонной кислоты, аскорбиновой кислоты, биотина, в кондитерской промышленности, для получения пищевого эталона и молочной кислоты. Формула глюкозы $\mathrm{C_6H_{12}O_6};$ общая формула углеводов $\mathrm{C_n(H_2O)_m}.$
2. На основании какого признака глюкозу относят к моносахаридам?
Глюкоза является моносахаридом потому, что не подвергается гидролизу, как, например, сахароза, мальтоза или крахмал.
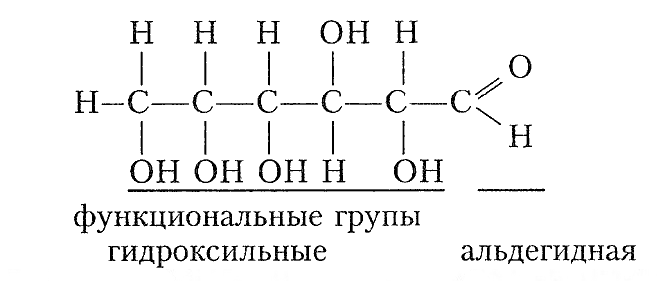
3. Запишите молекулярную формулу глюкозы и составьте структурную формулу глюкозы линейной формы. Укажите функциональные группы.
Молекулярная формула глюкозы $\mathrm{C_6H_{12}O_6}.$
Структурная формула:
4. В двух пробирках находятся растворы глюкозы и этанола. С помощью каких реакций можно определить, в какой из пробирок находится каждое из веществ?
Ярко-синяя окраска при приливании раствора глюкозы к гидроксиду меди (II) свидетельствует о том, что в составе молекул глюкозы содержится несколько гидроксильных групп, находящихся у соседних атомов, как в случае многоатомных спиртов.
С этанолом такая реакция не происходит.
5. Напишите уравнение реакции получения этанола из глюкозы. Приведите название реакции.
Спиртовое брожение глюкозы: $$\mathrm{C_6H_{12}O_6(дрожжи)\rightarrow 2C_2H_5OH+2CO_2\uparrow}$$
6. Рассмотрите структурные формулы уксусной и молочной кислот и укажите черты сходства и отличия в строении этих кислот. Как вы думаете, какими общими химическими свойствами могут обладать эти кислоты?

Общее: содержат одинаковые функциональные группы: $\mathrm{COOH}.$
Отличия: в молочной кислоте присутствует ещё одна функциональная группа — гидроксильная $\mathrm{OH}.$
Общие химические свойства: реакции с активными металлами, основными оксидами и щёлочи.
7. Составьте уравнения реакций синтеза глюкозы в природе и окисления ее в организме человека и сравните их. В чем состоит принципиальное различие этих реакций?
Синтез глюкозы в природе:
$\mathrm{6CO_2+6H_2O}\xrightarrow{hv,\,хлорофилл}\mathrm{C_6H_{12}O_6+6O_2\uparrow - Q}$
Окисление глюкозы в организме:
$\mathrm{C_6H_{12}O_6+6O_2\rightarrow CO_2\uparrow +6H_2O+Q}$
8. Рассчитайте химическое количество углекислого газа, который образуется при полном окислении глюкозы массой 133,2 г.
Дано: $m(глюкозы)=133.2\,г$
Найти: $n\mathrm{(CO_2)}-?$
Решение:
1) Определяем химическое количество глюкозы: $n=\dfrac{m}{M};$
$M_r=6A_r\mathrm{(C)}+12A_r\mathrm{(H)}+6A_r\mathrm{(O)}=$ $72+12+96=180;$
$M(глюкоза)=180\,г/моль;$
$n(глюкозы)=\dfrac{133.2\,г}{180\,г/моль}=0.74\,моль.$
2) Составляем уравнение реакции для определения химического количества углекислого газа:
$\mathrm{\overset{0.74\,моль}{\underset{1\,моль}{\underline{C_6H_{12}O_6}}}+6O_2\rightarrow \overset{x\,моль}{\underset{6\,моль}{\underline{6CO_2}}\uparrow} +6H_2O}$
$\dfrac{0.74}{1}=\dfrac{x}{6};$ $x=4.44\,моль.$
Ответ: $n\mathrm{(CO_2)}=4.44\,моль.$
9. В процессе спиртового брожения глюкозы массой 648 г получили этанол, который растворили в воде объемом 496,8 см$^3.$ Рассчитайте массовую долю этанола в растворе.
Дано:
$m(глюкозы)=648\,г\\
V\mathrm{H_2O)}=496.8\,см^2\\
или\,496.8\,г$
Найти: $\omega\mathrm{(C_2H_5OH)}-?$
Решение:
1) Определим химическое количество глюкозы:
$n=\dfrac{m}{M};$
$M_r=6A_r\mathrm{(C)}+12A_r\mathrm{(H)}+6A_r\mathrm{(O)}=$ $=72+12+96=180;$
$M(глюкозы)=180\,г/моль;$
$n(глюкоза)=\dfrac{648\,г}{180\,г/моль}=3.6\,моль.$
2) Составляем уравнение реакции для определения химического количества этанола:
$\mathrm{\overset{3.6\,моль}{\underset{1\,моль}{\underline{C_6H_{12}O_6}}}\xrightarrow{фермент}\overset{x\,моль}{\underset{2\,моль}{\underline{2C_2H_5OH}}}+2CO_2}$
$\dfrac{3.6}{1}=\dfrac{x}{2};$ $x=7.2\,моль.$
3) Определяем массу этанола:
$m=n·M;$
$M_r\mathrm{(C_2H_5OH)}=2A_r\mathrm{(C)}+6A_r\mathrm{(H)}+A_r\mathrm{(O)}=$ $24+6+16=46;$
$M\mathrm{(C_2H_5OH)}=46\,г/моль;$
$m\mathrm{(C_2H_5OH)}=7.2\,моль·46\,г/моль=331.2\,г.$
4) Определяем массовую долю $\omega =\dfrac{m}{m(раствора)};$
$\omega\mathrm{(C_2H_5OH)}=331.2\,г:(331.2+496.8)=0.4$ или $40\%.$
Ответ: $\omega\mathrm{(C_2H_5OH)}=40\%.$
10. Рассчитайте массу глюкозы, которая была подвергнута спиртовому брожению, если в реакции выделился газ таким же объемом (н. у.), как и в реакции уксусной кислоты массой 186 г с магнием, взятым в избытке.
Дано: $m\mathrm{(CH_3COOH)}=186\,г$
Найти: $m(глюкозы)-?$
Решение:
1) Определяем химическое количество кислоты:
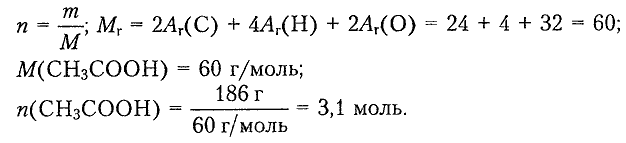
2) Составляем уравнение реакции для определения химического количества водорода:
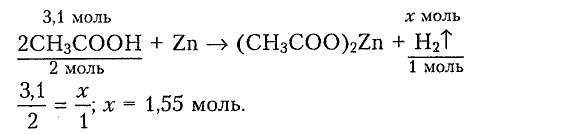
3) Составляем уравнение реакции для определения химического количества глюкозы:
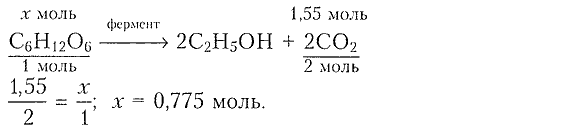
4) Определяем массу глюкозы:
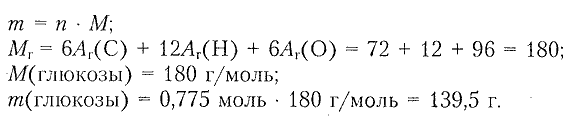
Ответ: $m(глюкозы)=139.5\,г.$